�����N�A�W���B
�� ���̃X���b�h�͉ߋ����O�q�ɂɊi�[����Ă��܂�
�s�������܂ގ_���}���K���W(A)������B���̏��x�����߂�B
�����T
�V���E�_�a��6.3g��500ml���X�t���X�R�ɓ���A�W���܂ŏ���������������(B)�B
�����Q
B50ml���z�[���s�y�b�g��p���ăR�j�J���r�[�J�[�ɂ͂���A3mol/l���_5ml��������A�R�j�J���r�[�J�[�����߂Ȃ���A
�r�����b�g�ɓ��ꂽ�J�}���K���T���J���E�����n�tC�œH�肵���Ƃ���C��16ml�H�������Ƃ���ŐԎ��F��悵���B
����3
B50ml���z�[���s�y�b�g��p���ăR�j�J���r�[�J�[�ɂ͂���3mol/l���_50ml����������AA��0.3g�����A�\���ɉ��߂��Ƃ���A
D,CO2�����������B
���̂��ƁA�r�����b�g�ɓ��ꂽ�J�}���K���T���J���E��C�œH�肵���Ƃ���C5.6ml�ŒW�ԐF��悵���B
1�A����3�Ŕ�������D�̑̐ς́H
2�AA�̏��x%�́H ���ʂ����q�ʂ��^�����Ă��Ȃ��̂ʼn����Ȃ��ȏ� ����̂��Ǝv�����炾�邢��������A�����ł�� 0.01mol/l�̃O���V�����n�t1L��0.1mol/l�_�������������Ă����Ɛ��n�t�͎_���ƂȂ�
�O��+�����O���} + H+ �@�͕��t�����Ɉړ�����̂ŃO��-�̑��݂͖����ł��A
�n�t���ɂ͎�ɃO��+�ƃO���}�����݂���ƍl������B
1�A0.01mol/l�̃O���V�����n�t1L��0.1mol/l�_40ml�������Ƃ���ph�́H
�������@��4.5�~10^-3�ł���B ��2=1.41
��3=1.73
log10 2=0.3
log10 3=0.48 �O���V���̂�͂��A�ɏn�t�����炳H+�͊_�̂�Ƃ��Ȃ�����ȁH
1040ml���Z���Čv�Z�����Ⴂ����̂��H
�܂����ꂶ�ᓚ���o�Ȃ����ǂ��B �_���}���K���̎�ނ��킩��Ȃ��̂ʼns�\�B ���A?�ɂȂ��Ă�ˁB
�_���}���K���S �ɂ����狳���Ă���A��̓I�ɂǂ����킩��Ȃ��H �O���V���͓����ł܂����I�I�I
�����ЂƂ^�₪�c
������Ԃ͂Ȃ�őo���C�I���X�^�[�g�ȂH
�������Ɏ_���ɂȂ�`���Ă����Ă��邯�ǂ��A�z�C�I���X�^�[�g�ōl���Ă�����Ԉ���Ă���B��[
>>16
�}���K���̂��1�̓�����ˁB���Ԃ����R�ɂȂ��Ă�B2�͂��Ԃ�1���o�����������͂� �����������Ǝ��₠���
�O���R�[�X�𐅂ɗn�����č���ɂȂ��Ă�Ԃ���4�ʂ̒Y�f���q�̂Ƃ�����]���ăK���N�g�[�X�ɂȂ����������Ƃ����Ȃ��́H ���ۂ͂قډ����Ă�͂������ǁA�Ȃ�����3�ŃV���E�_�����ׂĔ����������Ă킩��́H
�_���}���K���̕����S�Ĕ��������\���������ˁH�\���ʂƂ͏����ĂȂ��킯�����B
�܂����̏ꍇ�A�s�\�ɂȂ邯�ǂ��c ��������
(COOH)2��2CO2 + 2H+ + 2e-
�߃}���K���_�C�I���͗�
��������ӂ����킹���
2KMnO4 + 5(COOH)2 + H2SO4 �� 2MnSO4 + 8H2O + 10CO2
�ɂȂ���
���Ƃ͌v�Z����ˁH >>18
4�ʂ̒Y�f�͍��ɑS���W�Ȃ��Ȃ����H
�{���͎�������킩��ǃO���R�[�X�ƃK���N�g�[�X�͑S���ʂƍl���Ă邵�A����Ŏx��͑S���Ȃ��Ǝv����B >>19
��F����˂��́H����܂�l���ĂȂ����� >>21
�ƂȂ��Ȃ���������ˁH >>20
MnO2+ (COOH)2 = 2CO2 + Mn(OH)2
�ŁA
MnO2������0.3x/100/87
(COOH)2������5�~10^-3��
CO2�̑̐όv�Z����x������ȏ�V���E�_���S�Ĕ��������Ɖ��肵��������邯�ǁA�ǂ��ɂ��\���ʂ̃V���E�_�Ƃ͏����Ă��Ȃ��ȏ�A�_���}���K�����S�Ĕ�������\�������邭�Ȃ��H >>22
����͔�����̎c��̕����ł̎_���Ҍ������̘b�ł���H
���������c�ʂ킩��Ȃ��Ə��x�͉����Ȃ��͂���������ȑO�̖��ł���B >>24
�悭�ǂ�łȂ�����킩��Ȃ�����
��F���n�߂����������I���������߃}���K���_�J���E���̐F������
���Ă��Ƃ���Ȃ��� ��ŏ����Ă��ǂ�łȂ����炾�낤���ǂ��̖�蕁�ʂɓ����B >>23
���w�ِ��̓I�Ȃ��ʼnĂ���v���Ȃ������� �d���˂��ȁA���w�ŋ��i�j���C����������� >>24
�_���}���K��iv�ƃV���E�_�̔��������Ă�̂��H >>28
���A�A�A�A�ق�Ƃ�����������
�m���ɂ������� >>30
�q���g���Ȃ�����킩���B��������Ȏ����߂ď��������B�������W����1:2�ł��Ɠ����ł邩���͊Ԉ���ĂȂ��͂��ȂB >>32
������_���Ҍ��������Ǝv���A���M�͂Ȃ��� �t�H��Ȃ�_����̋�ʂ��c
�܂��ǂ����ɂ��뉴�͉����Ȃ��������c
�Ƃ肠�������x�����߂铙�����ꂩ���ˁH
���ꌩ����킩�邩������� MnO + 2CO2 + H2O���ĉ\��������� 1.6.3g�̓a���̕����ʂ����߂��1/20mol�ƂȂ�B500ml�̂���50ml�������Ɏg������50ml�̒��ɂ���V���E�_�̕����ʂ�1/200mol
2.�_���܂ƊҌ��܂̓d�q�̕����ʂ��l���Ď��𗧂Ă�Ɖ߃}���K���_�J���E���̃����Z�x��1/8mol/L�ƂȂ�
3�摜�̂��Ƃ����藧����MnO2�̕�����x�Ƃ���2���l�Ɏ��𗧂Ă��x=13/4�@�~�@10^-3
�����A�̏��x��(x�~103)/0.3
�v�Z�Ԉ���Ă���X�}�\
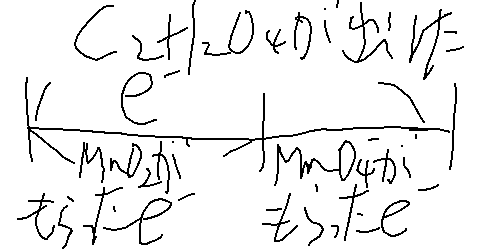 >>36
>>36
�t�H��͎_���Ҍ��ł������
�_���}���K��iv�ƃV���E�_�Ƃł̓d�q�Ɖ߃}���K���_�J���E���̓d�q���������Ȃ���Ă��Ƃ��Ǝv�����ǁA�ǂ����Ȃ̂��ȋ����Ă����Č����Ƃ��Ȃ���S�R�킩��˂���A���܂�ȁO�O �_���}���K���̔���������
MnO2+4H++2e-��Mn2++2H2O ����3�̓V���E�_�Ǝ_���}���K���Ŏ_���Ҍ�����
���̌�]�����V���E�_�Ɖ߃}���K���_�C�I���Ŏ_���Ҍ��������Ă邾������Ȃ���? �v�Z�����炨����������ǂ����ԈႦ�Ă�ۂ��� >>42
�������Ǝv�������ǂ킩��˂� MnO2�̕��q�ʂ�103����Ȃ���87�� >>47
����Ōv�Z������94�ɂȂ�������>>39��103�̕�����87�ɂ������ >>39
�ł���������CO2�������Ă邩�炻�̓������Đ��藧���H
�V���E�_�c���Ă���b�͕ʂ����Ǐ��ł��ĂȂ���CO2�̑̐ςƂ̐����������Ȃ����ǁc >>52
�܂�CO2�͏I����ĂȂ�����c
1/16�ɂȂ����̂͑����V���E�_1mol�ɑ���2mol�̓d�q���o��̂�Y��Ă�Ǝv�� >>54
���⏃���Ɋ���Z�~�X���Ă��킗������
�Ă������܂ŏo���Ȃ���������ł���
MnO2 + H2SO4 �� MnSO4 + 2H2O + 2CO2
����Ȃ��́H ���������ȂH�ǂ��l���Ă�78.4�ɂ����Ȃ�˂� >>53
������Ƒ҂��Ă悭�킩���
�V���E�_�������������ĂȂ�����߃}���K���_�J���E�������Ă�����_���Ҍ��������������킯��ˁH
�ݖ��CO2�̑̐ς͑���MnO2�����������������_�ł̘b���Ă�Ǝv�����ǁc�܂��Ƃ��ĂȂ�����킩��Ȃ����� >>55
���ꂾ��CO2�̑̐ς����߂��Ȃ����A��̐l���������������j�]���邭�ˁH
�������������Ă邩�炠�̓����������Ȃ͂��ȂB�������[��������ȁB ���Ȃ݂�CO2�̑̐ς͗L��������7.3�~10^-4L�ɂȂ�H >>58
H2SO4�̈Ӗ��Ƃ́c
���Ďv�������nj�œH�肵�Ă�̂� ���������Ă݂���94�D25=94������ ���_�͔����Ɋ֗^���Ȃ���
���_�̈Ӗ��͎_���������ɂ��邱��
�_����������Ȃ��Ɖ߃}���K���_�J���E���̎_����MnO2�Ŏ~�܂����Ⴄ���_���}���K���͂��������������Ȃ��Ȃ� >>58
���߂ӂɃV���E�_�����Y��Ă� >>61
�������̂͂��������v�Z�ԈႦ�Ă����ǂ���Ȃ�CO2��C�̔����S�̂ł̘b����
���ǂ�1/200mol�̃V���E�_�������I�����őS��CO2�ɂȂ�킯������CO2�̕����ʂ�1/100mol
���Ƃ�22.4�����邾�� >>65
�����c
D���čŏI�I�Șb���� >>65
��������AMnO2�̂Ƃ���KMnO4�̂Ƃ��Ŕ��������͍̂��킹��1.0�~10^-2������� >>65
�����͂��߂����v�����B�ł�����Ȃ�V���E�_���ł�����H
���������������Ȃ�A����ȍ~�̓H��ŏ�ɏ������������藧���Ȃ��ˁH �d�q�̂����������Ȃ��V���E�_�������Ă�킯�����B >>68
�V���E�_�̏��ł���^�C�~���O�͈�ԍŌ�̉߃}���K���_�J���E���ł̓H�肪�I�������Ƃ���������Ȃ��ˁH >>68
�V���E�_�S�������������
MnO2�Ƃ̔����Ŏc�����V���E�_���߃}���K���_�J���E���őS�����������Ă��ł���H�ԐF���o�Ă���܂œH�肵�Ă���Ă��Ƃ̓V���E�_�S��������������ł���
���߂�������r���N���Ă���������Ԉ���Ă��炲�߂� MnO2��3.25*10^-3mol,COOH2��5.0*10^-3mol�����炵�Ȃ� ����3�S�̂Ŕ�������co2�Ȃ�
����͖�蕶�̏��������킩��Â炢 MnO2�Ɣ������Ăł���CO2�Ȃ�0.15L��� �����܂ł킩���(1)�͂ł��邾��
���̈Ӗ����s��������������Ȃ��������� �� ���̃X���b�h�͉ߋ����O�q�ɂɊi�[����Ă��܂�


